- 日本 (Japan)
PulseSelect™
パルスフィールドアブレーションシステム
PulseSelect™ パルスフィールドアブレーション(PFA)システムは、アブレーションと検査の両機能を備えたPulseSelect PFA Loopカテーテルと、パルス電圧を送出するためのPulseSelect PFAジェネレータによって主に構成される、心房細動(AF)治療用のアブレーションシステムです。
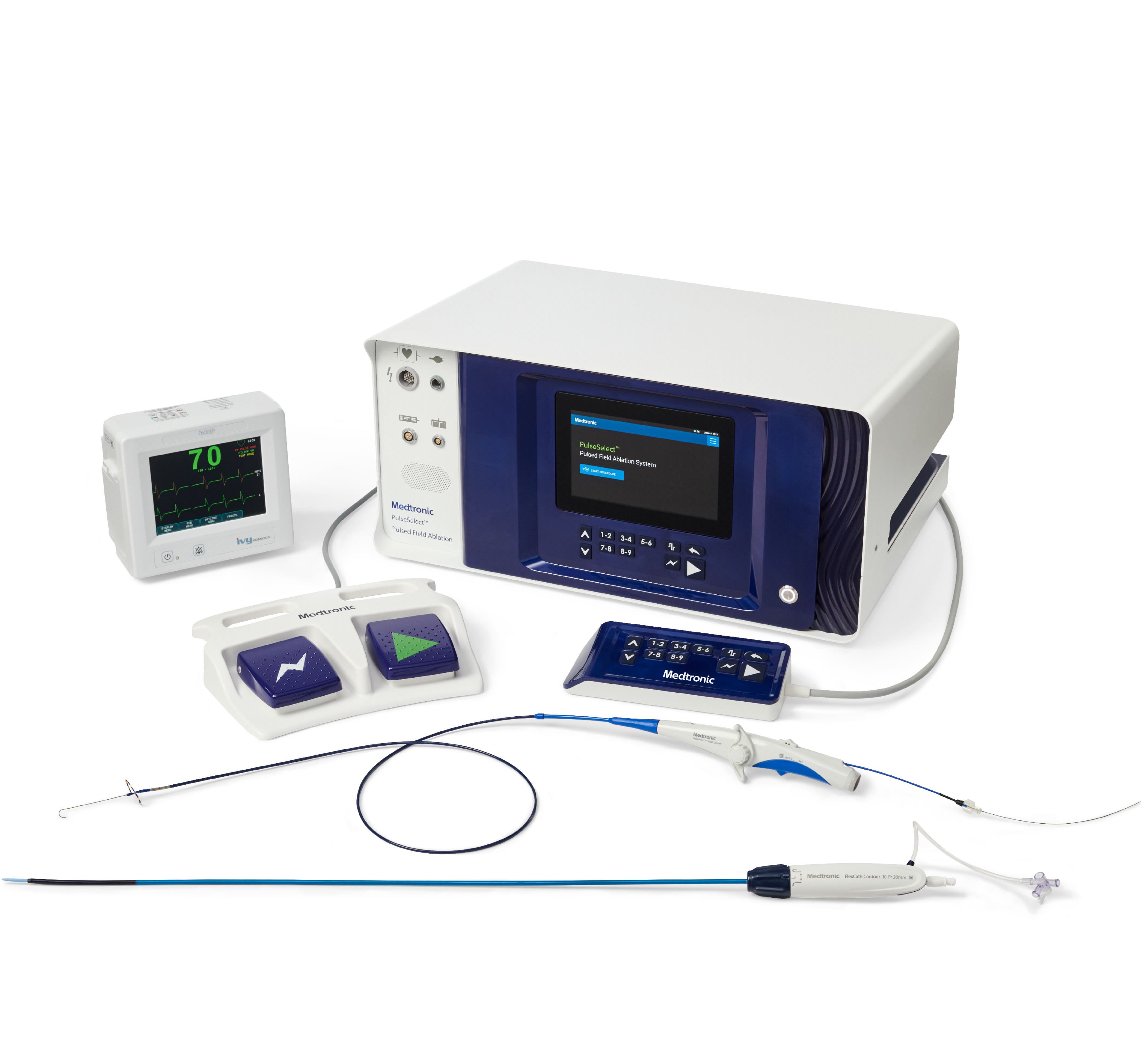
概要
Setting the standard in safety
PulseSelect™ パルスフィールドアブレーションシステムは、15年以上にわたるPFA研究を経て開発されており、独自の安全機能を搭載しています。
PulseSelect PFA Loopカテーテルは、薬剤抵抗性の再発性症候性発作性AFの治療、及び薬剤抵抗性の症候性持続性AFの治療を目的としたカテーテルです。パルス出力発生装置であるPulseSelect PFAジェネレータから、カテーテルに双極性二相性パルス列を送出し、電極周囲に電場(パルスフィールド)を形成します。このパルスフィールドが細胞に作用を及ぼし、細胞膜に不可逆な孔を形成することでリージョンを形成します(不可逆的電気穿孔法)。心筋細胞は、食道や横隔神経、肺静脈を構成する細胞に比べて、パルスフィールドに対する影響を受けやすいことが知られています1。PFAでは、この差を利用することで、心筋組織に対して選択的にリージョンを形成し、食道や横隔神経、肺静脈といった周辺組織に関する合併症の発生リスクを低減することが期待されています。
製品特徴
PulseSelect™ PFAジェネレータ
- 安全なエネルギー送出のための過電流自動検知機能
- 心電図モニタから入力されたR波に同期してエネルギー送出可能な機能
- 横隔神経に対する近接性評価のためのテストパルス機能

PulseSelect™ PFA Loopカテーテル
- 9極の電極(素材:金)によりアブレーション・心内心電図の検出・診断用ペーシング刺激の送出が可能
- 環状電極アレイ径:25mm
イリゲーション:不要 - シャフト外径:9Fr
屈曲:バイディレクショナル

固定化された電極間隔2
電極周囲に安定した電場領域を形成

20度の前方傾斜デザイン2
電極アレイ全体の均一な組織コンタクトをサポート

オーバーザワイヤ型デザイン2
安定したカテーテル配置と、セルフセンタリング機能によるPVに対する同軸性の確保をサポート

試験データ
PULSED AF試験1
PULSED AF試験は、発作性AFおよび持続性AF治療におけるPulseSelect™ PFAシステムの安全性と有効性を評価するため、日本を含む9か国において実施された国際共同IDE(Investigational Device Exemption;治験医療機器適用免除)試験です。
パルスフィールドアブレーションに関する国際共同治験において、初めて日本国内施設が参加しました。2024年2月までに実施された心房細動アブレーションIDE試験の中でも低い、主要安全性事象発生率0.7%を示しています。
0.7%
主要安全性事象※の
発生率
(術後6か月時点)
70%
発作性AF
AF/AFL/AT非発生率
(術後12か月時点)
62%
持続性AF
AF/AFL/AT非発生率
(術後12か月時点)
※主要有害事象は、脳血管障害が1件、心タンポナーデ/穿孔が1件であった。
関連情報
カテーテルアブレーション製品
Medtronic Times
メドトロニックのニュースレターです。弊社製品・イベントや学術関連・臨床試験等の情報をご案内させていただきます。是非ご登録ください。
新規登録 (opens new window)Reference
Verma A, Haines DE, Boersma LV, et al. Pulsed Field Ablation for the Treatment of Atrial Fibrillation: PULSED AF Pivotal Trial. Circulation. May 9, 2023;147(19):1422–1432.
Medtronic data on file. November 2023.
販売名/医療機器承認番号
PulseSelect PFA Loopカテーテル / 30600BZX00082000
PulseSelect PFAジェネレータ / 30600BZX00083000
販売名/ 製造販売届出番号
PulseSelect PFAアクセサリ / 13B1X00261C00005
使用目的又は効果、警告・禁忌を含む使用上の注意等の情報につきましては製品の電子添文をご参照ください。
